Les actualités de la journée du Jeudi 16 fevrier
CancerTV
 Uro-Onco
Uro-Onco

Résultats TALAPRO-2 et PROpel : Parpi et NHT : une combinaison pour tous?
17 février 2023
Article
 Uro-Onco
Uro-Onco
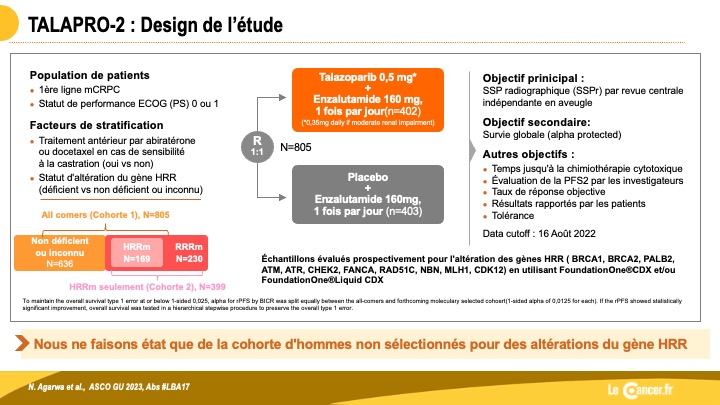
TALAPRO-2: combinaison enzalutamide + talazoparib en 1ère ligne de résistance à la castration… Un pas de plus vers l’association NHT + PARPi pour tous !?
17 février 2023
Peut-être bien que oui… L’étude de phase 3 TALAPRO-2, à son tour, a évalué l’efficacité de l’association du talazoparib (Talazo) […]
Lire la suite
Article
 Uro-Onco
Uro-Onco
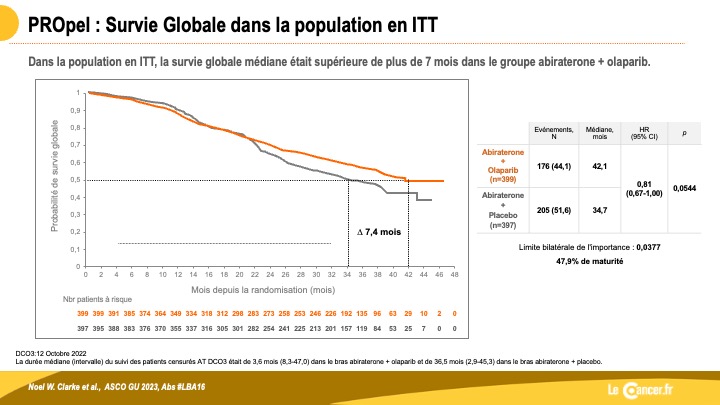
2- Données de survie globale de l’étude PROPEL… il ne manque pas grand-chose !
17 février 2023
Bien que le bénéfice soit plus marqué en cas d’anomalie HHR (HRR+ : HR 0.50 [IC95 0.34-0.73] vs HRR- : HR 0.76 […]
Lire la suite
CancerTV
 Uro-Onco
Uro-Onco

Résultats de l’étude PEACE-1. Comment traiter le sujet âgé ?
17 février 2023
TÉLÉCHARGEZ LE POSTER ICI
Lire la suite
Article
 Uro-Onco
Uro-Onco
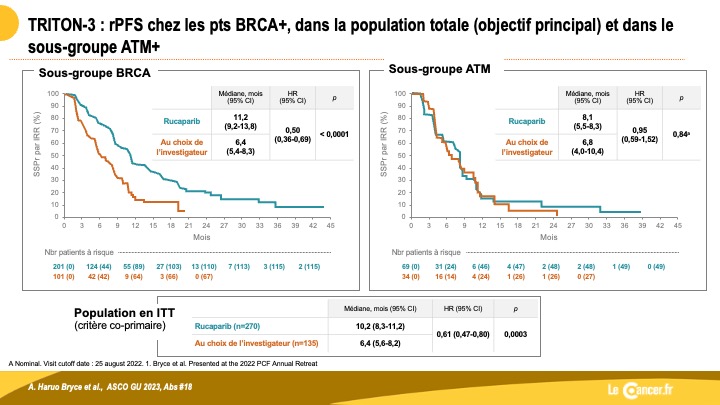
Le rucaparib plus fort que le docetaxel ou une NHT en 2è ligne et + dans le CPRCm avec anomalie BRCA ou ATM.
17 février 2023
Le rucaparib (Ruca) est également approuvé au US sur la base des résultats de l’étude de phase 2 TRITON-2 (Abida, […]
Lire la suite
Article
 Uro-Onco
Uro-Onco

Faut-il intensifier la radio-hormonothérapie (RT-HT) de rattrapage après prostatectomie radicale (PR) et PSA dosable?
17 février 2023
L’étude randomisée FORMULA-509 a évalué l’ajout de 6 mois d’AAP plus APA à la RH-HT chez des patients avec un […]
Lire la suite
Article
 Uro-Onco
Uro-Onco
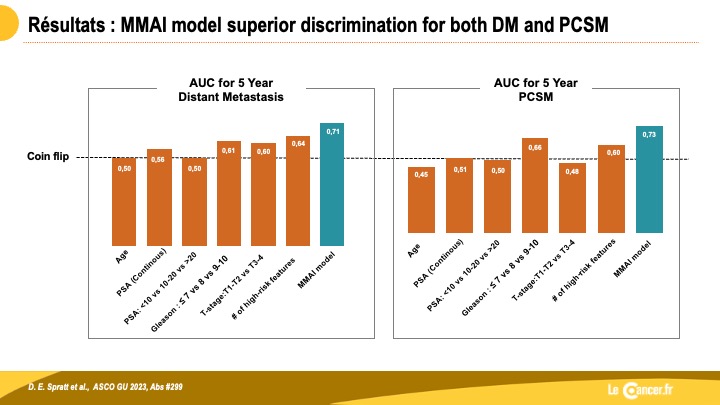
Un modèle d’intelligence artificielle (MMAI) affine le risque pronostique des patients avec un cancer de prostate (CP) localisé à haut/très haut risque.
17 février 2023
Récemment, un biomarqueur pronostique MMAI, ArteraAI Prostate, a été formé et validé dans le CP localisé pour stratifier avec plus […]
Lire la suite
Article
 Uro-Onco
Uro-Onco
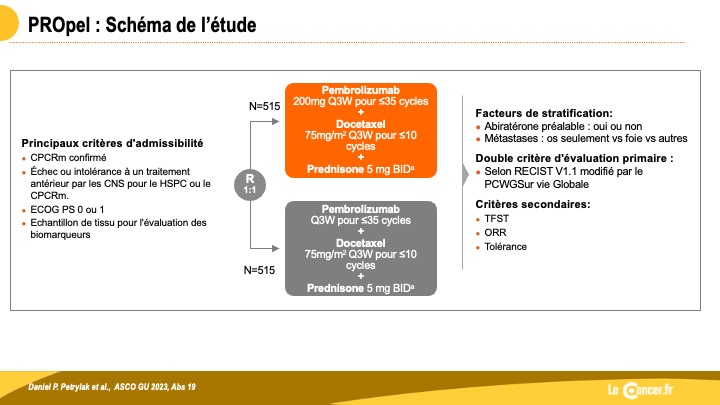
Immunothérapie et Cancer de prostate : Pressentiment confirmé: encore une combinaison à base de docetaxel qui va rejoindre la longue liste des essais de phase 3 négatifs.
17 février 2023
Le docetaxel reste depuis bientôt 2 décennies « le » traitement de référence dans les cancers de la prostate résistant à la […]
Lire la suite
Article
 Uro-Onco
Uro-Onco
Actualisation de l’étude MAGNITUDE : Confirmation des données avec un suivi médian de 26.8mois
17 février 2023
Les données de l’étude MAGNITUDE ont été communiquées en 2022 avec des résultats positifs en SSPr dans la population de […]
Lire la suite
CancerTV
 Uro-Onco
Uro-Onco

Session prostate : Actualités en radiothérapie au stade localisé et à la rechute biochimique.
17 février 2023
Article
 Uro-Onco
Uro-Onco
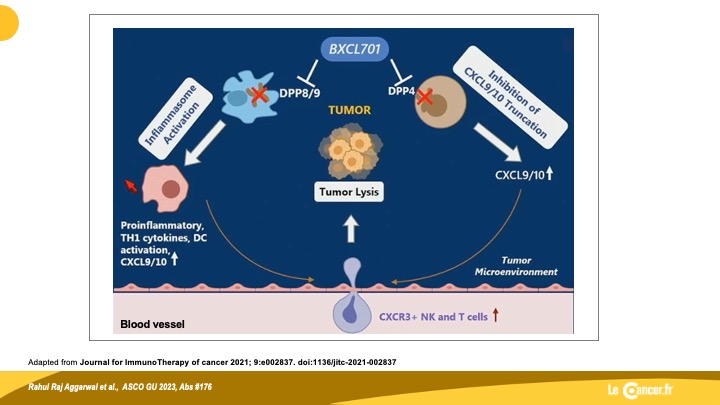
Cancer de la prostate neuroendocrine à petite cellules : Un espoir est il possible ?
17 février 2023
Malgré les avancées thérapeutique de ces dernières années les carcinomes prostatiques neuroendocrines à petites cellules représentent encore et toujours un […]
Lire la suite
Article
 Uro-Onco
Uro-Onco

Efficacité du darolutamide (DARO) en association avec la déprivation androgènique (ADT) et le docetaxel (DOC) en fonction du volume tumoral et du risque de la maladie dans l’étude de phase 3 ARASENS.
17 février 2023
L’effet de l’ajout du DARO sur la SG était cohérent dans les sous-groupes préspécifiés, y compris les maladies métastatiques de […]
Lire la suite