Les actualités de la journée du 11 Sept
Article
 Sein/Gynécologie
Sein/Gynécologie
DATA : Données finales !
11 septembre 2022
L’essai de phase III DATA étaient donc mené chez des patientes ménopausées avec un cancer du sein localisé RH+, en […]
Lire la suite
Article
 Sein/Gynécologie
Sein/Gynécologie
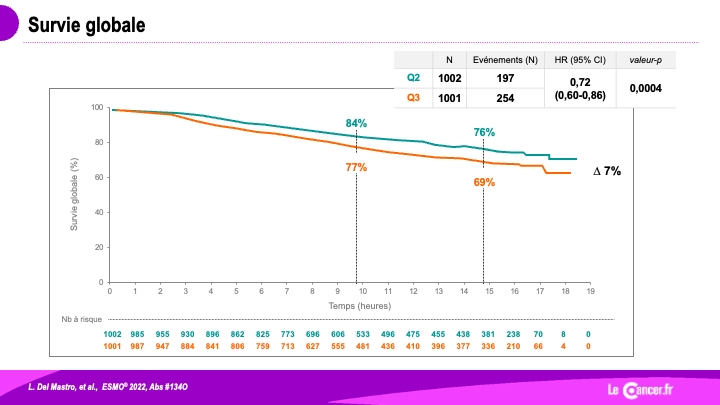
Données finales du schéma de chimiothérapie dose-dense dans les cancers du sein localisés
11 septembre 2022
L’essai GIM 2 est un essai randomisé en plan factoriel 2×2 qui pose 2 questions : L’intérêt d’un schéma d’anthracyclines dose-dense […]
Lire la suite
CancerTV
 Sein/Gynécologie
Sein/Gynécologie

Le Ki67 comme biomarqueur dynamique de l’hormonothérapie néoadjuvante.
11 septembre 2022
Article
 Sein/Gynécologie
Sein/Gynécologie
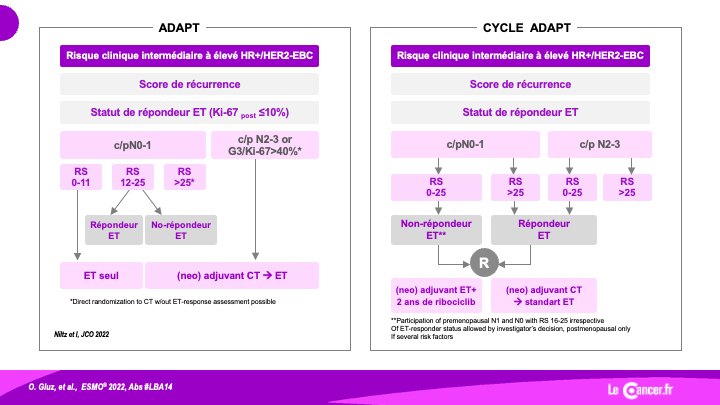
ADAPT : Impact de l’âge, du recurrence score et de la suppression ovarienne sur l’efficacité d’une hormonothérapie d’induction.
11 septembre 2022
Les essais ADAPT utilise pour la décision d’une chimiothérapie adjuvante (CT) un autre marqueur pronostique (outre l’âge et le score […]
Lire la suite
Article
 Sein/Gynécologie
Sein/Gynécologie
Pourrait-on remplacer la chimiothérapie par une bi-immunothérapie dans les cancers du sein triple négatifs localisés ?
11 septembre 2022
L’intérêt des inhibiteurs de points de contrôle de type anti-PDL1 dans les cancers du sein triple négatif localisés a été […]
Lire la suite
Article
 Sein/Gynécologie
Sein/Gynécologie
N’est pas immunosensible qui veut !
11 septembre 2022
Courageusement, Kyte et al (Oslo University Hospital), ont exploré l’apport d’une double immunothérapie par ipilumumab – nivolumab à une chimiothérapie […]
Lire la suite
Article
 Sein/Gynécologie
Sein/Gynécologie
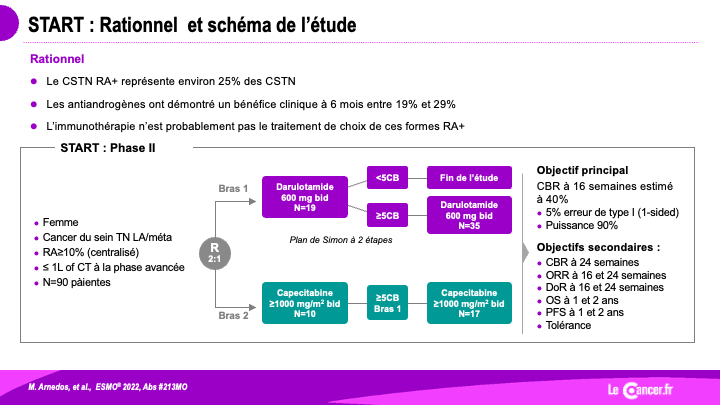
Cancers du sein triple négatifs : le chemin est encore long…même quand c’est lent !
11 septembre 2022
Au nom du groupe sein d’UNICANCER, M. Arnedos a présenté les premiers résultats très attendus de l’essai START, mené dans […]
Lire la suite
Article
 Sein/Gynécologie
Sein/Gynécologie
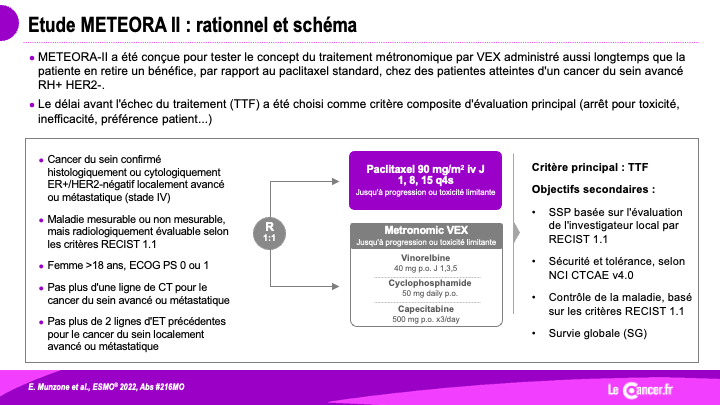
Il faut toujours se hâter lentement !
11 septembre 2022
Cet essai de l’IBCSG a randomisé 1:1 un schéma paclitaxel hebdomadaire (90 mg/m² J1-8-15/28) versus une polychimiothérapie métronomique (VEX) associant […]
Lire la suite