Les actualités de la journée du 4 juin
Article
 Digestif
Digestif
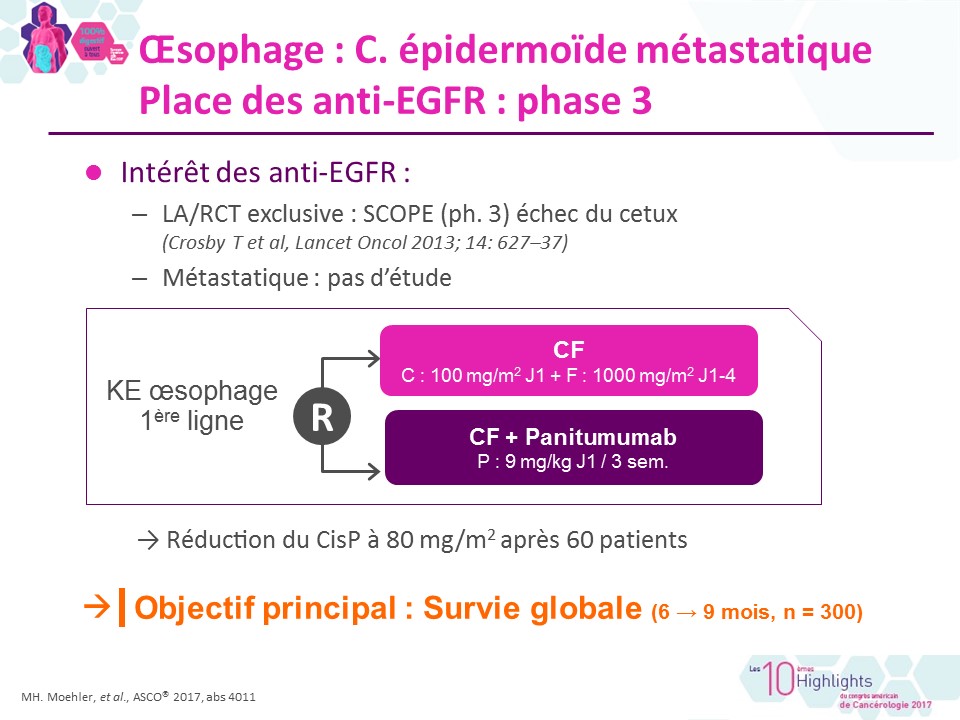
Cancers de l’œsophage : la place des anti-EGFR revisitée
4 juin 2017
Deux situations complémentaires font l’objet d’études présentées ce jour : En situation métastatique (pour les carcinomes épidermoïdes) : Dans l’étude allemande […]
Lire la suite
Article
 Digestif
Digestif
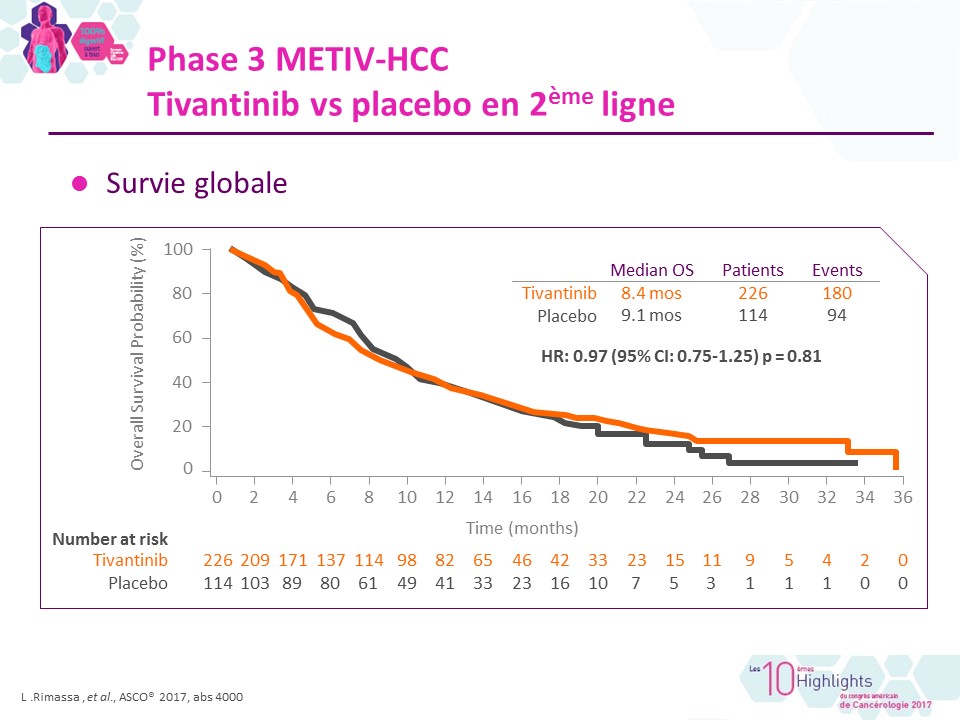
Inhibition de Met dans le CHC : le tivantinib échoue en 2ème ligne
5 juin 2017
Au total, 340 patients Child A avec PS 0-1 ont été randomisés selon un ratio 2:1 pour recevoir le Tivantinib […]
Lire la suite
Article
 Digestif
Digestif
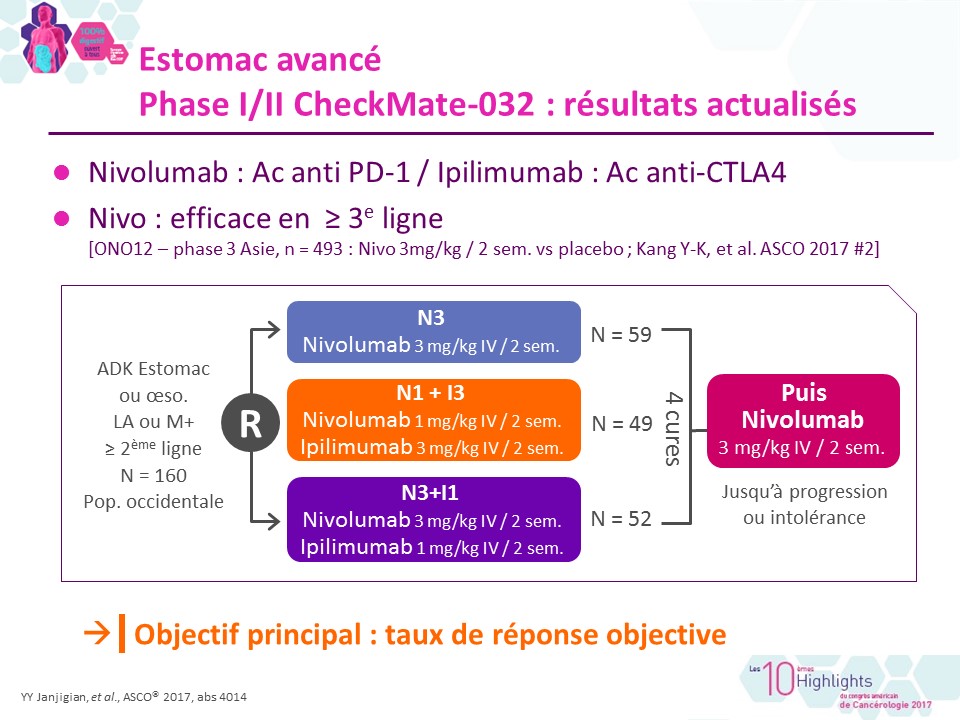
Immunothérapie et cancer gastrique
5 juin 2017
Monothérapie anti-PD1: actualisation des résultats de la cohorte 1 KEYNOTE-059 (#4003) avec 259 patients traités en 3ème ligne ou […]
Lire la suite
Article
 Digestif
Digestif
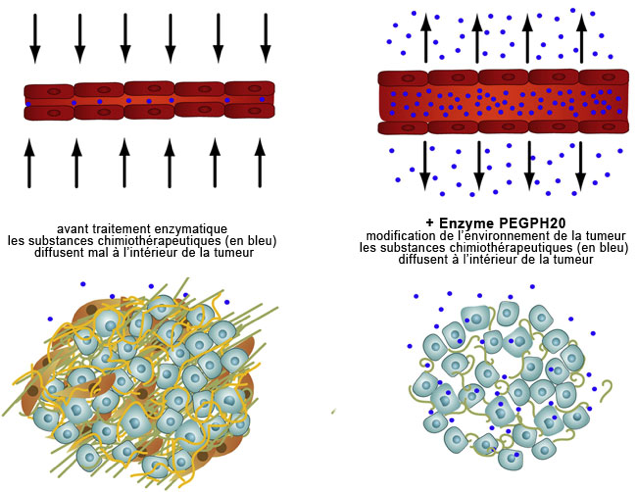
Cancers de pancréas : le stroma tumoral ciblé par une hyaluronidase pégylée.
5 juin 2017
L’étude randomisait des patients atteints d’adénocarcinome pancréatique métastatique, non traités préalablement, entre une chimiothérapie par gemcitabine + nab-paclitaxel avec ou […]
Lire la suite
CancerTV
 Digestif
Digestif

BILCAP : quand la Capécitabine passe le cap sans se faire de bile!
5 juin 2017
Cet essai, dont les résultats ont été rapportés à l’ASCO GI 2017, n’a pas montré de supériorité du GEMOX […]
Lire la suite
Article
 Digestif
Digestif
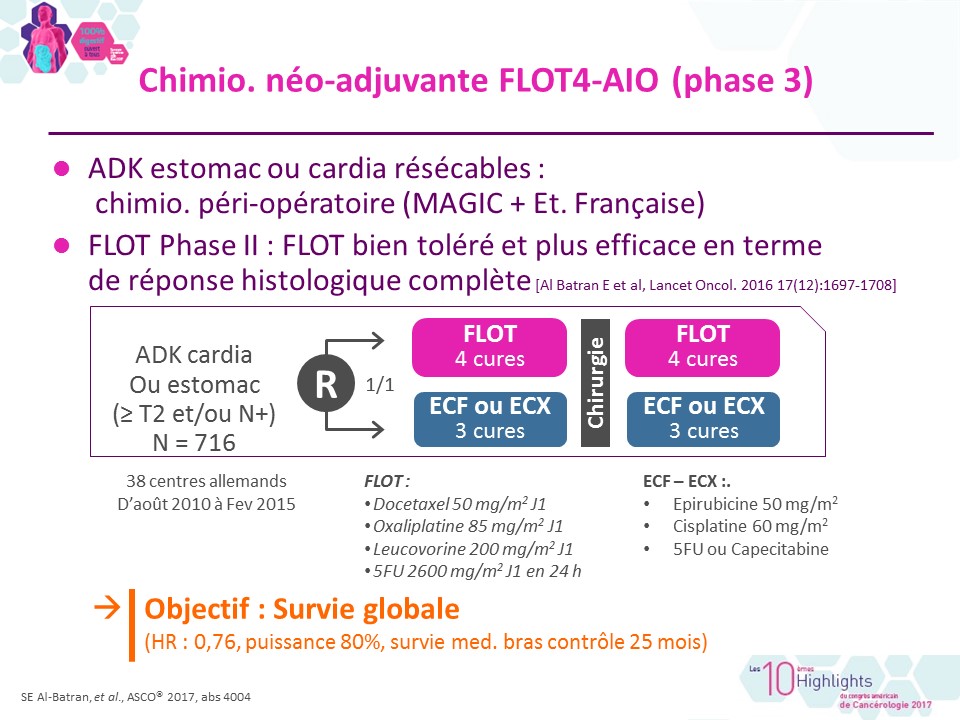
FLOT4 : nouveau standard de chimiothérapie péri-opératoire des adénocarcinomes gastriques et du cardia résécables
5 juin 2017
L’étude allemande de phase 3 (n = 716) « FLOT4 » a évalué l’intérêt du schéma FLOT (Taxotère + Oxaliplatine – 5FU) […]
Lire la suite
CancerTV
 Digestif
Digestif
Article
 Digestif
Digestif
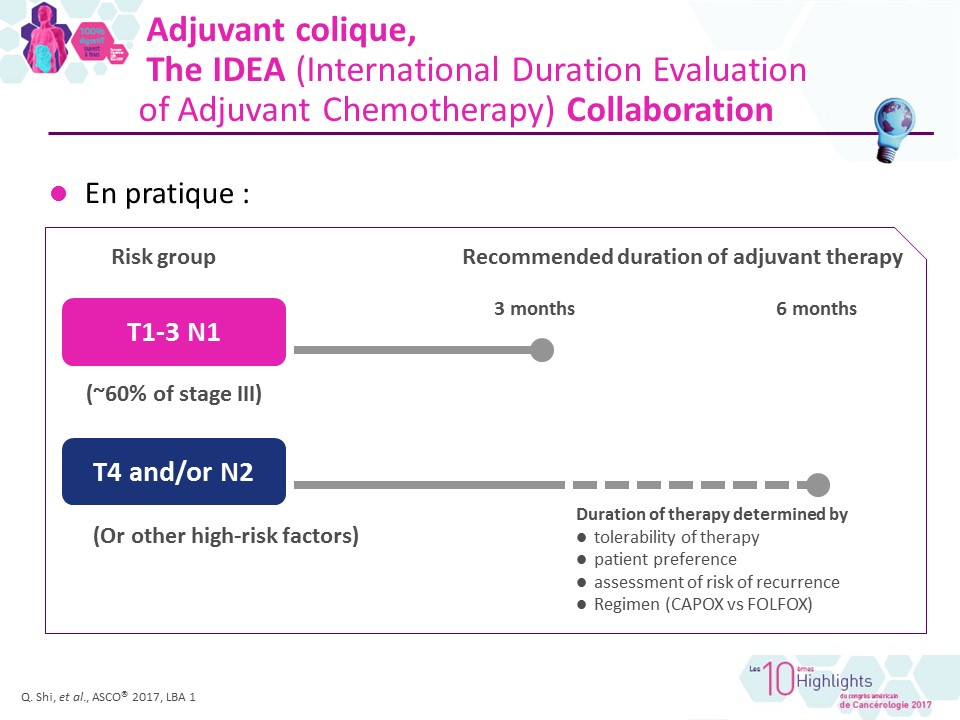
Traitement adjuvant des cancers coliques, et pourquoi pas 3 mois ? Quelle bonne idée !
5 juin 2017
Raccourcir à 3 mois la durée de traitement pourrait sérieusement diminuer le risque de toxicité neurologique lié au traitement, simplifier […]
Lire la suite