Les actualités de la journée du Lundi 3 juin
Article
 Digestif
Digestif
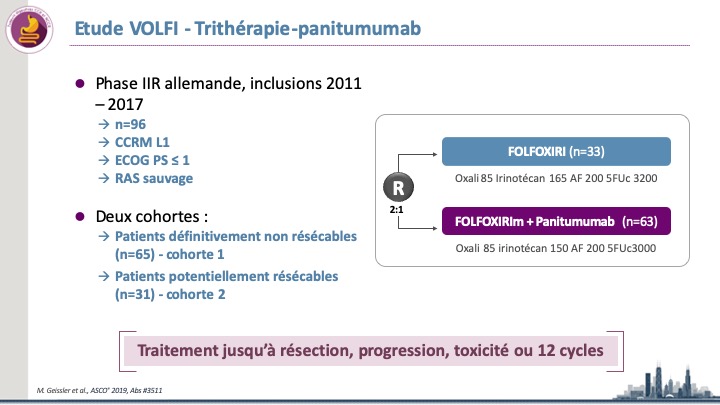
Cancer colorectal métastatique avec RAS sauvage : Trithérapie plus panitumumab, résultats finaux de l’étude VOLFI.
4 juin 2019
Cette étude testait une triple chimiothérapie plus ou moins panitumumab en première ligne des CCRM Ras sauvage. Les résultats déjà […]
Lire la suite
CancerTV
 Digestif
Digestif

Interview_Dr Cindy Neuzillet, Institut Curie, Paris
4 juin 2019
Une première thérapie ciblée dans les cancers du pancréas métastatique avec mutation germinale de BRCA, et les honneurs […]
Lire la suite
CancerTV
 Digestif
Digestif
Article
 Digestif
Digestif
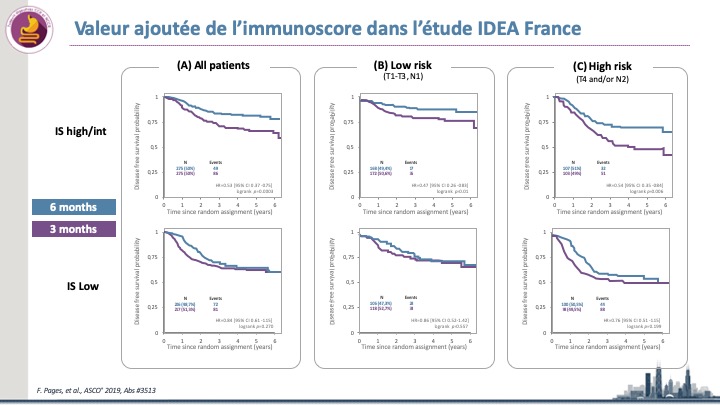
Cancers coliques de stade III : Valeur pronostique et prédictive de l’Immunoscore dans l’étude IDEA France.
4 juin 2019
L’IS était considéré comme élevé chez 9.4% des patients, intermédiaire chez 47% et faible chez 43%. La valeur pronostique pour […]
Lire la suite
Article
 Digestif
Digestif
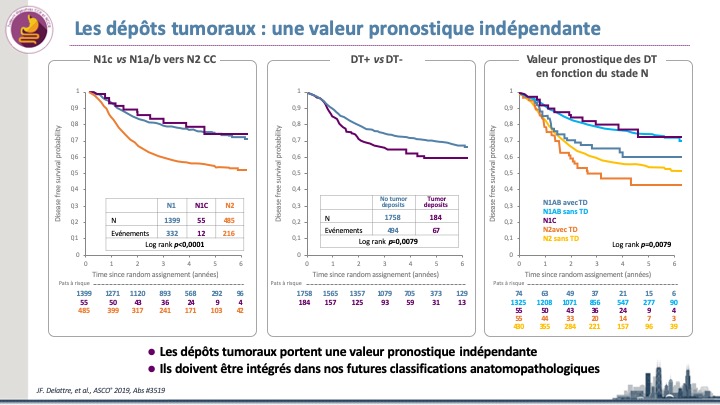
Les dépôts tumoraux en cas de cancer colique de stade III: un marqueur de mauvais pronostic sous-estimé !
4 juin 2019
Ils sont classés pN1c dans la dernière classification TNM si il n’y a pas de ganglion métastatique mais ne sont […]
Lire la suite
Article
 Digestif
Digestif
ADN tumoral circulant après résection d’un cancer colique : une forte valeur pronostique !
4 juin 2019
Sur les 485 patients opérés (tumeurs stade II ou III) un ctDNA a été retrouvé dans 12% des cas. (et […]
Lire la suite
Article
 Digestif
Digestif
Comment rendre les CCRM MSS sensibles à l’immunothérapie ?
4 juin 2019
L’étude canadienne CO26 visait à évaluer une double inhibition PDL1 et CTLA-4 face à des soins palliatifs seuls en […]
Lire la suite
Article
 Digestif
Digestif
Du côté de la chirurgie, ça bouge aussi à l’ASCO !
4 juin 2019
Une étude chirurgicale japonaise a voulu étudier un dogme non remis en cause depuis 60 ans, celui de la […]
Lire la suite
Article
 Digestif
Digestif
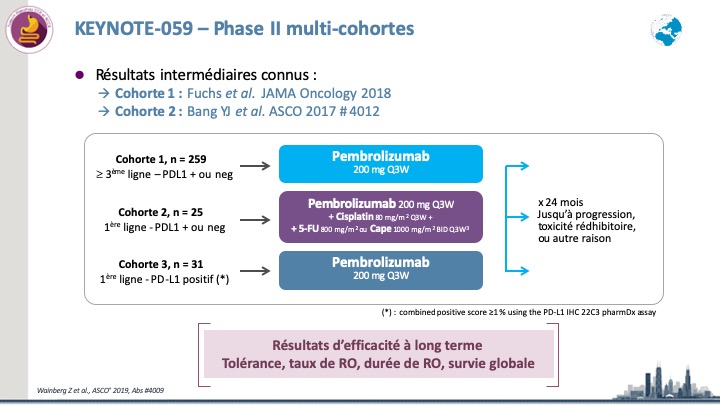
Cancer gastrique avancé : le pembrolizumab omniprésent (Etude KN-059 et KN-062)
4 juin 2019
Les résultats actualisés de l’étude KN-059 (phase II) ont été présentés. Cette étude comportait 3 cohortes : – Cohorte 1 […]
Lire la suite
Article
 Digestif
Digestif

Cancers de l’œsophage avancés : le pembrolizumab bien positionné en deuxième ligne (Keynote 181)
4 juin 2019
Dans cette étude internationale de phase III, 628 patients ont été randomisés (dont 401 C. épidermoïdes) entre pembrolizumab et une […]
Lire la suite
Article
 Digestif
Digestif
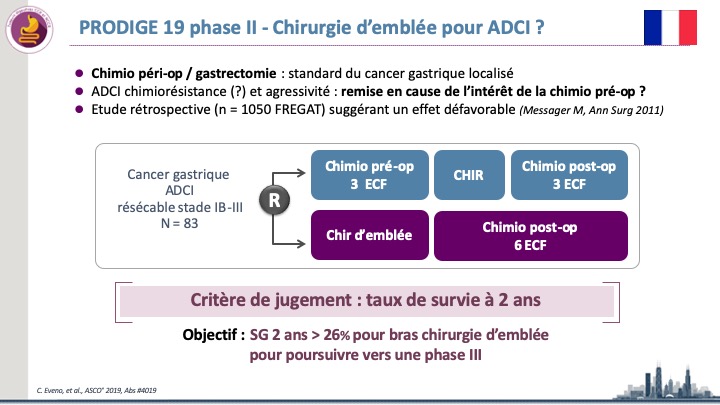
Adénocarcinome à cellules indépendantes : la chimiothérapie périopératoire demeure le standard.
4 juin 2019
L’étude de phase II Prodige 19 a permis d’inclure 83 patients (dans 27 centres français) porteurs d’un adénocarcinome gastrique de […]
Lire la suite
Article
 Digestif
Digestif
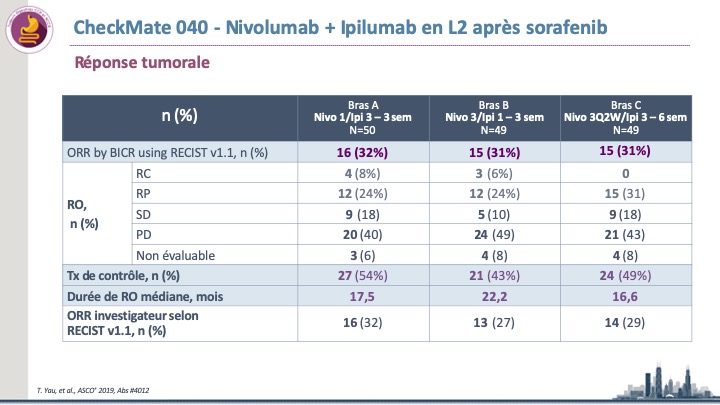
CHC avancé après échec du sorafenib : l’impressionnante association Nivolumab/ Ipilimumab (Essai CheckMate 040).
4 juin 2019
Un total de 148 patients a été randomisé en 3 bras: -bras A (Nivo 1 mg/kg + Ipi 3 mg/kg/3 […]
Lire la suite
Article
 Digestif
Digestif
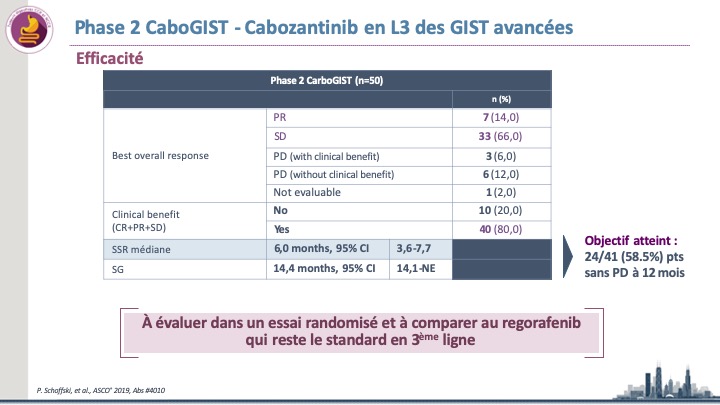
Le cabozantinib fait son entrée en 3ème ligne des GIST avancées (Essai CaboGIST)
4 juin 2019
Des données pré-cliniques ont suggéré que cet ITK pourrait réverser la résistance à l’imatinib secondaire à l’activation de la voie […]
Lire la suite